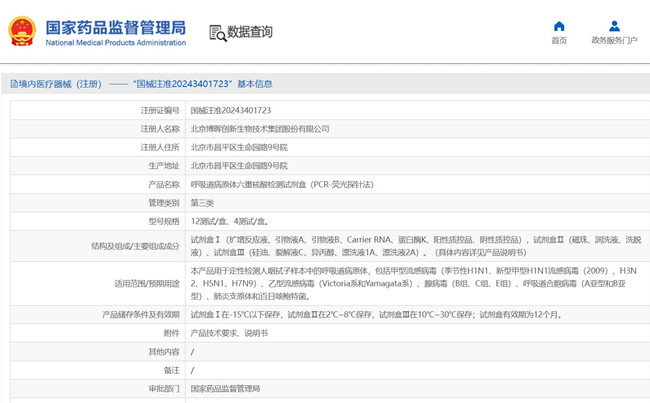
呼吸道病原體六重核酸檢測試劑盒(PCR-熒光探針法)在我國屬于第三類體外診斷試劑產品�����,產品用于定性檢測人咽拭子樣本中的呼吸道病原體����,包括甲型流 感病毒、乙型流感病毒(Victoria 系和 Yamagata 系)��、腺病毒(B 組��、 C 組�����、E 組)、呼吸道合胞病毒(A 亞型和 B 亞型)�、肺炎支原體和百日咳鮑特菌����。
引言:呼吸道病原體六重核酸檢測試劑盒(PCR-熒光探針法)在我國屬于第三類體外診斷試劑產品���,產品用于定性檢測人咽拭子樣本中的呼吸道病原體��,包括甲型流
感病毒(季節性 H1N1�、新型甲型 H1N1 流感病毒(2009)�、H3N2、H5N1��、
H7N9)��、乙型流感病毒(Victoria 系和 Yamagata 系)、腺病毒(B 組、
C 組�����、E 組)��、呼吸道合胞病毒(A 亞型和 B 亞型)�����、肺炎支原體和百
日咳鮑特菌。本文為大家帶來呼吸道病原體六重核酸檢測試劑盒(PCR-熒光探針法)臨床試驗設計實例,一起看正文����。
一���、呼吸道病原體六重核酸檢測試劑盒(PCR-熒光探針法)主要原材料
本產品在制備過程中主要原材料包括 Carrier RNA����、磁珠�����、引物�����、
探針、擴增反應液、含 FluA�、B 假病毒���、RSV 假病毒����,AdV 假病毒�、
M.P 質粒��、B.P 質粒和 HEK293 細胞的混合液����。其中 Carrier RNA、磁
珠���、引物、探針�����、擴增反應液��、FluA�����、B 假病毒、RSV 假病毒,AdV
假病毒��、M.P 質粒���、B.P 質粒為外購��,HEK293 細胞為申請人自行生產����。
申請人對主要原材料進行了供應商的選擇�����,通過功能性試驗,篩
選出合格供應商��,制定了各主要原材料的質量標準并經檢驗合格�����。
企業參考品和質控品的設置情況
本產品企業參考品包括陽性參考品��、陰性參考品、檢測限參考品
和精密度參考品����。參考品均采用病原體培養物制備而成����。組成如下:
陽性參考品:20 份�����,由試劑盒檢測位點各個基因型別的病原體培
養物組成�。
陰性參考品:10 份�,由試劑盒檢測范圍外的病原體培養物組成。
精密度參考品:3 份��,由中強陽性��、弱陽性和陰性濃度水平的病
原體培養物組成����。
檢測限參考品:20 份��,由包含試劑盒檢測位點各個基因型別的最
低檢測限濃度水平的病原體培養物組成
二��、呼吸道病原體六重核酸檢測試劑盒(PCR-熒光探針法)穩定性研究
申請人對本產品的效期穩定性、凍融穩定性�、運輸穩定性以及樣
本穩定性進行研究,確定了在各種條件下本產品及樣本的有效保存時
間。
效期穩定性:使用企業參考品對三批試劑按照技術要求檢測,分
別于試劑盒保存的第 0 個月����、6 個月�、10 個月����、12 個月、15 個月進行
穩定性試驗;檢測結果均符合技術要求���。因此,試劑盒按照說明書要
求可保存 12 個月,檢測性能穩定�。
三�、呼吸道病原體六重核酸檢測試劑盒(PCR-熒光探針法)臨床試驗設計實例
申請人在首都兒科研究所附屬兒童醫院�、廣州醫科大學附屬第三
醫院和濟南市兒童醫院共 3 家機構完成了臨床試驗����。
入組人群為呼吸
道感染的患者�����,樣本類型為咽拭子��。
針對甲型流感病毒、乙型流感病毒����、腺病毒����、呼吸道合胞病毒和肺炎支原體核酸檢測�����,臨床試驗采用試驗體外診斷試劑與已上市同類產品進行比對,入組病例 2150 例。
針對甲型流感病毒,納入陽性病例 263 例,陰性病例 1887 例。試驗結果顯示�����,陽性符合率為 98.1%(95CI:95.6%����,99.2%),陰性符
合率為 99.3%(95CI:98.8%,99.6%)���;
針對乙型流感病毒,納入陽性病例 212 例,陰性病例 1938 例����。試驗結果顯示����,陽性符合率為 100%(95CI:98.2%�,100%),陰性符合
率為 99.5%(95CI:99.1%,99.8%);
針對腺病毒,納入陽性病例 277 例����,陰性病例 1873 例����。試驗結果顯示���,陽性符合率為 96.4%(95CI:93.5%�,98.0%),陰性符合率為
99.7%(95CI:99.4%�����,99.9%)���;
針對呼吸道合胞病毒�,納入陽性病例 224 例�,陰性病例 1926 例。
試驗結果顯示���,陽性符合率為 99.6%(95CI:97.5%,99.9%)����,陰性
符合率為 99.2%(95CI:98.7%����,99.5%)����;
針對肺炎支原體,納入陽性病例 251 例��,陰性病例 1899 例���。試驗
結果顯示,陽性符合率為 98.8%(95CI:96.5%�,99.6%)�,陰性符合率為 99.3%(95CI:98.8%��,99.6%)��。針對百日咳鮑特菌核酸檢測,臨床試驗采用試驗體外診斷試劑與
Sanger 測序進行比較研究����,共入組 2150 例病例����,包括陽性病例 352
例���,陰性病例 1798 例��。試驗結果顯示,陽性符合率為 99.7%(95CI:
98.4%���,99.9%),陰性符合率為 99.8%(95CI:99.5%��,99.9%)����。同
時還進行了與百日咳鮑特菌培養鑒定的比較,包括培養陽性病例 85
例�,培養陰性病例 810 例��。靈敏度為 98.8%(95CI:93.6%,99.8%)�,特異度為 70.1%(95CI:66.9%�����,73.2%)。針對與培養鑒定不一致的
樣本���,均結合 Sanger 測序進行了確認。
如有體外診斷試劑臨床試驗設計及數據統計服務需求���,歡迎您隨時方便與杭州證標客醫藥技術咨詢有限公司聯絡,聯系人:葉工�,電話:18058734169����,微信同�����。